Les fondamentaux – Chapitre 7 – Échographie
F. Patat et M. Ronot
Plan du chapitre
- Notion d’onde mécanique
- Principes de l’échographie
- Bases sémiologiques du mode B
- Modes Doppler
- Agents de contraste échographiques
- Bases technologiques
- Conclusion
Objectifs
Les objectifs de ce chapitre sont de présenter les techniques ultrasonores en allant de la compréhension des principes physiques jusqu’aux bases sémiologiques des images obtenues. Dans ce parcours, il est nécessaire d’aborder la nature des interactions des ondes ultrasonores avec les tissus du corps humain et les bases techniques du fonctionnement des systèmes employés aujourd’hui. Ce descriptif est délibérément court et limité à la stimulation de l’intuition des phénomènes, sans calcul donc, hormis la connaissance de l’unité géométrique du champ acoustique, à savoir la longueur d’onde. La description des principaux modes Doppler qui, aujourd’hui, font partie de tout examen approfondi est également envisagée. Une synthèse des caractéristiques de l’échographie et les perspectives d’évolution des outils ultrasonores en médecine clôtureront ce chapitre.
Notion d’onde mécanique
Les ondes mécaniques sont des phénomènes très fréquents : les sons dans l’air, les vagues à la surface de l’eau, les tremblements de terre ou les vibrations d’une corde instrumentale. Pour en donner une définition plus générale et abstraite, on considère un milieu matériel quelconque (solide, liquide ou gazeux), au repos pour simplifier ; il est possible de modifier localement la position d’une partie du milieu par l’application de forces. Cette perturbation de l’équilibre local engendrera des forces de voisinage qui créeront alors un mouvement. Ce phénomène de déplacements induits de proche en proche est décrit par le concept d’onde mécanique sous-tendu par un autre mot clé, celui de propagation. Lorsque les ondes mécaniques peuvent être perçues par l’ouïe d’un être vivant sous forme de sons, on parle d’ondes acoustiques. L’acoustique est donc la science qui étudie les sons.
Propriétés du milieu de propagation
Certaines propriétés dites « mécaniques » du milieu conditionnent la façon dont les ondes s’y propagent. Une onde entraîne des déformations du milieu qui mettent en jeu ses différentes propriétés élastiques intrinsèques. Pour désigner ces propriétés, on utilise le terme de « module ». Dans un milieu isotrope, toutes les directions sont équivalentes ; il n’existe que deux modules élastiques indépendants : en compression (changement de volume mais pas de forme) et en cisaillement (changement de forme).
Les modules élastiques s’expriment en Pascal (Pa) ; ils correspondent à la contrainte mécanique nécessaire pour obtenir une certaine déformation. Pour définir le module élastique en compression, on utilise le coefficient K qui gouverne la loi de la pression P nécessaire pour obtenir un changement relatif donné de volume V :
ΔP= -K * ΔV / V
La variation relative de volume est bien ΔV / V et le signe – nous indique que, pour une pression positive, ΔP, on obtient bien une diminution de ce volume. K est le coefficient de proportionnalité entre la contrainte mécanique (la pression) et la déformation obtenue.
Pour l’eau, K = 2,25 GPa = 2,25 109 Pa. Il faut une pression de 22,5 MPa pour comprimer un volume d’eau de 1 %. C’est la pression qui règne par exemple à une profondeur de 2250 mètres.
La dynamique de la mise en mouvement de la matière dépend de son inertie, c’est-à-dire de sa masse volumique ρ. Pour l’eau, on a ρ = 1000 kg/m3. On définit, enfin, une caractéristique essentielle du milieu vis-à-vis des ondes : la vitesse de propagation, aussi appelée célérité. Il faut bien distinguer la célérité, qui est la vitesse du phénomène « onde », et la vitesse des molécules du milieu. Prenons l’exemple des vagues sur la mer : un objet flottant, qui représente le mouvement des molécules d’eau, a un mouvement essentiellement vertical, montant et descendant au passage des vagues. Celles-ci, en revanche, se propagent horizontalement beaucoup plus vite. La célérité d’une onde est rapide si le milieu a une forte élasticité, c’est-à-dire s’il est raide, difficile à déformer. Inversement, elle est plus lente si le milieu présente une masse volumique importante. On démontre que la célérité c est déterminée par célérité2 = coefficient élastique/masse volumique soit :
c2 = K / ρ
La célérité du son dans l’air vaut 340 m/s et correspond au mur du son en aéronautique. Dans l’eau, elle est encore plus importante et vaut 1500 m/s, soit 5400 km/h : le son d’un caillou jeté dans le port de Brest pourrait en théorie s’entendre à New York une heure plus tard ! Les caractéristiques intrinsèques du milieu que sont ses coefficients élastiques et sa masse volumique déterminent la célérité des ondes ultrasonores.
On distingue les ondes à polarisation transverse où le mouvement est perpendiculaire à la direction de propagation (c’est typiquement le cas avec notre exemple du bouchon flottant et des vagues) et les ondes à polarisation longitudinale où le déplacement de matière est parallèle au vecteur de propagation. Les ondes habituellement utilisées en échographie sont des ondes de compression qui se propagent dans des milieux (les tissus biologiques) dont la consistance est proche de celle de l’eau ; il s’agit d’ondes longitudinales.
Les ondes de cisaillement ne sont pas utilisées en échographie conventionnelle. Le module de cisaillement peut toutefois être utilisé afin de déterminer la « dureté » (rigidité) d’une zone prédéfinie. On parle d’élastographie ultrasonore. En effet, la vitesse de propagation des ondes de cisaillement est directement reliée à la rigidité du milieu. La mesure de cette vitesse est réalisée selon des modalités différentes de celles utilisées en échographie conventionnelle. Il s’agit d’une technologie d’introduction plus récente, mais qui se généralise.
On définit par ailleurs une autre quantité importante appelée impédance acoustique qui est le produit de la masse volumique par la célérité de l’onde : Z = ρ·c. Nous verrons plus loin en quoi Z est une caractéristique déterminante dans le comportement des ondes acoustiques lorsqu’elles changent de milieu. L’unité donnée à Z est le Rayl (1 Rayl = Pa· s/m) en hommage au grand physicien britannique J.W. Rayleigh (1842–1919), fondateur de l’acoustique moderne. Le tableau 7.1 donne les caractéristiques de l’air et de l’eau.
Tableau 7.1 – Propriétés mécaniques de l’air et de l’eau à 25 °C.
|
Milieu |
Masse volumique (kg ∙ m–3) |
Coefficient élastique (Pa) |
Célérité (m/s) |
Impédance Z (Rayl) |
|
Air |
1,3 |
1,5 105 |
340 |
442 |
|
Eau |
1000 |
2,25 109 |
1500 |
1,5 106 |
Ondes sinusoïdales
De nombreuses formes temporelles peuvent se propager sous forme d’onde. Un type fréquent dans la nature et très commode sur le plan mathématique est représenté par les fonctions sinusoïdales. Une telle onde pourra être décrite par la formule suivante où l’on décrit la pression p qui dépend à la fois du temps t et de la distance x :
p(X,t) = A ⋅ sin [2 π { (x/λ) – (t/T) } ] = A ⋅ sin [2π/λ V⋅ (x – c ⋅t)] = A ⋅ sin [2 π f { (x/c) – t } ]
A est l’amplitude, f la fréquence, T la période et λ la longueur d’onde. Le motif de l’onde se répète à intervalle régulier dans le temps – c’est la période T – et à intervalle régulier dans l’espace : il suffit de photographier le phénomène pour voir λ, la longueur d’onde. Le lien entre ces grandeurs est facile à retrouver : au bout d’un temps T, l’onde voyageant à la vitesse c se sera déplacée de la quantité c·T = λ. On a par ailleurs : T = 1/f et c = λ·f.
À noter que le signe – entre les variables temporelles et spatiales implique une propagation dans le sens des x positifs ; le signe + inverserait le sens (figure 7.1).
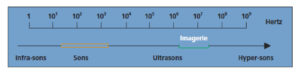
Représentation sur l’échelle des fréquences des principaux domaines des ondes mécaniques.
Chez les humains, les sons sont définis par la gamme de fréquences audibles par un sujet jeune, typiquement 20 Hz à 20 kHz. Au-delà, on parle d’ultrasons et les fréquences essentiellement utilisées en imagerie médicale sont dans la gamme 2 MHz à 20 MHz, ce qui correspond à des périodes temporelles entre 500 et 50 ns. Il est important d’avoir en tête les longueurs d’onde dans les tissus mous où la célérité est très proche de celle de l’eau ; une onde à 1,5 MHz dans un milieu où c vaut 1500 m/s a une longueur d’onde de 1 mm :
λ = c / f = {1500 m⋅s-1} / {1,5⋅106 s-1} = 10-3 m
Une onde de 15 MHz aura une longueur d’onde dix fois plus petite, soit un dixième de millimètre. Cette notion de longueur associée à l’onde est essentielle car c’est l’étalon selon lequel doivent être analysés tous les phénomènes subséquents, notamment les interactions ultrasons-tissus. C’est aussi le juste ordre de grandeur de la résolution que l’on peut attendre des images échographiques.
L’amplitude des ondes acoustiques peut s’exprimer dans différentes variables comme la pression p de l’onde (à ne pas confondre avec la pression ambiante du milieu qui est fixe) ou la vitesse v des molécules du milieu. On peut d’ailleurs noter que ces quantités sont proportionnelles et que le coefficient qui les relie est précisément l’impédance acoustique Z.
On a ainsi p = Z·v de la même manière qu’en électricité la loi d’Ohm U = R·I traduit le lien entre tension électrique et courant, la résistance R étant le coefficient de proportionnalité reliant ces deux grandeurs.
Propriétés acoustiques des tissus
Les propriétés acoustiques des tissus biologiques sont résumées dans le tableau 7.2. On voit très clairement sur ce tableau que l’ensemble de ce qu’on appelle les tissus mous en échographie, c’est-à-dire tous les organes, à l’exception du squelette et des organes à contenu gazeux, possèdent une impédance acoustique voisine de 1,6 MRayl et une célérité à peine supérieure à celle de l’eau. Cela reflète le fait que nos tissus contiennent une grande quantité d’eau et que, mécaniquement, à l’échelle des ondes ultrasonores, ils se comportent comme un milieu liquide épais aqueux très riche en lipides, protéines et glucides. Toutes ces molécules, essentielles à la vie, changent peu la masse volumique et la faible compressibilité (due à l’eau) de ces milieux. De façon similaire, la gamme des célérités des ondes acoustiques dans les tissus mous est assez restreinte au voisinage de 1550 m/s. Cette situation est extrêmement favorable et permet aux faisceaux d’ultrasons d’avoir des trajectoires presque droites, comme on va le découvrir ensuite. Il est important aussi de noter que ces propriétés, célérité de l’onde et impédance acoustique, sont indépendantes de la composition fréquentielle de l’onde propagée.
Tableau 7.2 – La célérité en m/s et l’impédance acoustique Z de différents milieux du corps humain.
|
Tissu |
Célérité (m/s) |
Z : impédance (MRayl) |
|
Air |
340 |
0,0004 |
|
Eau |
1480 |
1,48 |
|
Poumon |
650 |
0,06-0,26 |
|
Sang |
1566 |
1,65 |
|
Os cortical |
3000–4000 |
4,2-8 |
|
Foie |
1560 |
1,65 |
|
Graisse |
1450 |
1,38 |
|
Muscle |
1550–1630 |
1,65-1,74 |
|
Rein |
1570 |
1,65 |
|
Cerveau |
1550 |
1,6 |
|
Peau |
1600 |
1,84 |
|
Polyamide |
2340 |
2,9 |
Atténuation
Schématiquement, l’intensité d’une onde acoustique se modifie (le plus souvent diminue) au cours de sa propagation ; on parle d’atténuation. Deux phénomènes en rendent compte : l’absorption et la dispersion.
Pour traiter de l’absorption, il faut se souvenir qu’une onde acoustique transporte de l’énergie à la fois sous forme cinétique (avec la vitesse des molécules mises en mouvement) et sous forme potentielle (avec l’énergie élastique de déformation du milieu). Comme tout mouvement, ceux induits par le passage de l’onde entraînent des frottements et une partie de l’énergie est ainsi soustraite sous forme de chaleur. C’est le phénomène d’absorption qui contribue largement à atténuer l’énergie des faisceaux ultrasonores utilisés. Classiquement, la part d’énergie absorbée est proportionnelle à l’énergie en transit ; on retrouve donc la loi classique dans bien des domaines (optique ou rayons X) d’atténuation exponentielle. Si x est la distance parcourue et I(x) l’intensité au point d’abscisse x, alors où α est le paramètre d’atténuation dont la dimension est l’inverse d’une longueur, en cm–1 par exemple.
Deux points sont importants à retenir :
- aux fréquences qui nous intéressent en échographie, le coefficient α est assez élevé ; les faisceaux sont rapidement absorbés lorsqu’ils atteignent les régions anatomiques profondes. Les échographes comportent donc des systèmes d’amplification puissants pour les signaux rétrodiffusés distants ;
- dans les tissus, le coefficient α est proportionnel à la fréquence : α = β·f et comme il intervient dans l’exposant de l’exponentielle, l’accroissement de la fréquence augmente sensiblement l’absorption.
Il serait théoriquement préférable de réaliser des explorations échographiques à la plus haute fréquence possible de manière à utiliser de courtes longueurs d’onde, interagissant à une échelle très fine avec l’anatomie tissulaire et permettant ainsi d’obtenir les meilleures résolutions spatiales possibles. La recherche d’un compromis est nécessaire car les plus hautes fréquences sont trop vite absorbées. Cela explique pourquoi elles sont réservées à l’exploration des tissus superficiels. Concrètement, on utilise des sondes de basse fréquence pour explorer des organes profonds (bonne pénétration des ondes au prix d’une résolution spatiale moindre), a fortiori pour des patients en surpoids, et des sondes haute fréquence (excellente résolution spatiale mais absorption rapide) pour les investigations superficielles ou endocavitaires.
En ce qui concerne la dispersion, nous verrons ensuite qu’il est possible de manipuler les faisceaux ultrasonores ; ceux-ci sont rarement des ondes planes (c’est-à-dire des plans se propageant de façon perpendiculaire à la direction de propagation), mais plus souvent des ondes divergentes ou convergentes. L’énergie totale de l’onde, constante, se répartit ainsi sur des surfaces d’onde qui varient au cours de la propagation. Dans une zone où l’onde est divergente, la surface d’onde s’accroît et l’intensité locale diminue. Inversement, il est possible, comme nous le verrons dans le paragraphe « Bases technologiques », de focaliser les faisceaux, c’est-à-dire de concentrer l’énergie au voisinage d’un point focal. On peut par ce biais augmenter l’intensité locale.
Il faut retenir que, pour les appareils diagnostiques, l’absorption est, de loin, le phénomène dominant.
Interface entre milieux de propagation
Les variations intratissulaires d’impédance acoustique conditionnent la manière dont une onde ultrasonore interagit avec ce tissu. Ces interactions peuvent être catégorisées en considérant trois phénomènes : la transmission, la réflexion et la diffusion.
Considérons la situation schématisée sur la figure 7.2. Deux milieux de célérités différentes c1 et c2 sont séparés par une interface plane. Chacun des milieux étant homogène, les ondes acoustiques se propagent en ligne droite mais, à l’interface, les équations de propagation ne peuvent plus être satisfaites par une seule onde. Il se passe le même phénomène qu’en optique ; deux ondes supplémentaires par rapport à l’onde incidente prennent naissance : une onde réfléchie et une onde transmise, appelée aussi onde réfractée.
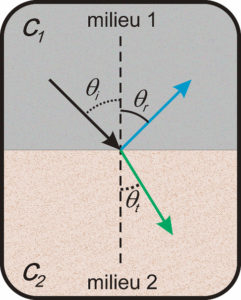
Interactions à l’interface de deux milieux (1 et 2) de célérité différente (c1 et c2).
Onde incidente (flèche noire), réfléchie (flèche bleue) et transmise (flèche verte) avec leur angle par rapport à la normale : θi, θr et θt.
Les valeurs de célérité gouvernent les lois des angles θ selon les lois de Snell-Descartes : θi = θr et c2· sin θi = c1· sin θt.
Remarque : Si sin θi ≥ c1/c2, il y a réflexion totale, c’est-à-dire une absence d’onde transmise.
Les célérités des milieux gouvernent les angles de réflexion et réfraction. En revanche, ce sont les impédances qui vont conditionner la puissance des ondes réfléchies et réfractées. Prenons le cas plus simple d’une incidence normale à l’interface (figure 7.3).
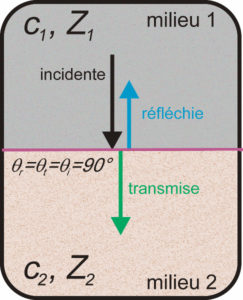
Deux milieux de caractéristiques acoustiques différentes séparés par une interface plane avec un triplet d’ondes incidente, réfléchie et transmise perpendiculaires à l’interface.
Si on définit par R et T les coefficients de réflexion et de transmission :
- R = puissance de l’onde réfléchie/puissance de l’onde incidente ;
- T = puissance de l’onde transmise/puissance de l’onde incidente.
Les lois de continuité à l’interface permettent de montrer que :
R = (Z1 – Z2)2 / (Z1 + Z2)2
et
T = (4 · Z1 · Z2) / (Z1 + Z2)2
On peut vérifier que R + T = 1, ce qui est logique puisque la puissance incidente est totalement répartie entre le faisceau transmis et le faisceau réfléchi.
La réflexion aux interfaces peut devenir très importante si les impédances sont très différentes et, dans ce cas, l’énergie transmise peut être considérablement réduite. C’est le cas des interfaces entre la sonde et l’air, puis entre l’air et la peau du patient. Pour éviter des pertes considérables à ces deux interfaces, il est nécessaire d’appliquer un gel entre la sonde et la peau du patient. Les fortes différences d’impédance entre tissus mous et air et entre tissus mous et os expliquent aussi l’impossibilité des explorations échographiques si le faisceau rencontre l’os ou des structures contenant des gaz (poumon, tube digestif).
L’interface plane a une surface très grande comparée à la longueur d’onde. Considérons maintenant le cas opposé d’un milieu constellé de petites hétérogénéités d’impédance dont la forme importe peu, puisqu’elles sont très petites à l’échelle de l’onde acoustique incidente, c’est-à-dire en comparaison avec sa longueur d’onde (figure 7.4).

Diffusion d’onde plane (en bleu) par une collection d’hétérogénéités d’impédance (en jaune).
Chacune des hétérogénéités est la source d’une microréflexion. Elle donnera lieu à une onde secondaire de forme sphérique, car issue d’une origine quasi ponctuelle. Ces ondes sphériques ainsi engendrées en très grand nombre sont incohérentes si les sources sont dispersées aléatoirement dans l’espace. Le faisceau incident est ainsi transformé en un ensemble d’ondelettes incohérentes sans direction privilégiée. Ce phénomène appelé diffusion est familier en optique (c’est l’explication du brouillard ou de l’aspect des nuages qui sont des assemblages de microgouttelettes d’eau liquide en suspension qui diffusent la lumière visible). Les tissus des organes observés en échographie sont constitués de cellules qui contiennent des noyaux ayant une plus grande impédance acoustique, séparées par de nombreuses interfaces entre elles et avec la microvascularisation, les fibres des tissus de soutien, etc. Chacune de ces microstructures contribue ainsi au caractère plus ou moins diffusant d’une région échographique.
Principes de l’échographie
Le principe sur lequel repose l’échographie est celui de l’écholocalisation. Il est utilisé, on le sait, dans le monde animal, notamment par les chauves-souris et certains mammifères marins. Le Sound Navigation And Ranging (SONAR), qui est une invention du XXe siècle, repose sur le même principe. Il a tout d’abord été utilisé à des fins militaires dans la guerre sous-marine, puis a été diffusé aux domaines de la pêche et du monde médical après 1945.
Ligne échographique
En échographie, tout commence avec la production d’ondes ultrasonores pulsées de courte durée, typiquement une période de la fréquence centrale, transmises au patient par la face avant de la sonde.
Le schéma de la figure 7.5 montre un système d’émission-réception d’onde ultrasonore pulsée. L’émetteur est ce que l’on appelle une sonde (à gauche du schéma). La sonde est tenue dans la main lorsque l’on réalise un examen échographique. Il en existe de très nombreux modèles, ayant des tailles et des formes différentes. Ces caractéristiques permettent de produire des ondes à des fréquences variées. Elles ont toutes en commun de pouvoir à la fois émettre et recevoir des ondes acoustiques et les transformer en signaux électriques. L’onde émise est supposée voyager sous forme d’un faisceau assez fin le long de la ligne pointillée en rouge. L’émission est pulsée sur le plan temporel (représentée par l’onde rouge sur le schéma). En pratique, elle oscille brièvement pendant une ou deux périodes, puis est stoppée. La sonde, après avoir émis l’onde initiale, se place en mode « écoute » et enregistre tous les signaux qui viennent frapper sa surface sensible. L’onde émise voyage (vers la droite sur le schéma) au sein du milieu à explorer et engendre, lorsqu’elle rencontre une rupture d’impédance acoustique, un couple onde réfléchie-onde transmise, comme nous l’avons vu. L’onde réfléchie retourne alors vers la sonde. On parle alors d’écho (qui donne son nom à l’échographie). L’onde transmise poursuit, quant à elle, son trajet dans la même direction, mais avec une puissance moins grande. La perte de puissance est faible si les ruptures d’impédance acoustique sont faibles, ce qui est souvent le cas dans les tissus mous. L’énergie qu’elle transporte peut ainsi provoquer de nouveaux échos en raison des contrastes d’impédance situés un peu plus loin en profondeur. Ces échos sont recueillis par la sonde après un délai t qui dépend de la durée du trajet aller-retour de l’onde ultrasonore. Si la source de l’écho est à la profondeur d, celui-ci arrivera avec le retard 2 d/c par rapport à l’instant d’émission. La détection d’un écho permet donc d’en déduire la profondeur à laquelle il a été généré. En écoutant suffisamment longtemps, la sonde recueille plusieurs échos successifs, générés à des profondeurs croissantes. Ainsi, avec une seule émission d’onde, on peut obtenir des renseignements sur l’anatomie acoustique le long de toute une ligne.
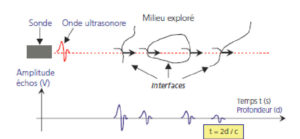
Schéma d’émission-réception d’une onde pulsée mettant en évidence l’interaction de l’onde transmise avec le milieu exploré.
En dessous, le diagramme amplitude-temps délais montre les délais d’arrivée des échos croissant avec la profondeur.
À noter que ces échos sont de moins en moins puissants en raison des phénomènes d’atténuation que subit l’onde durant son trajet aller puis retour. Des amplificateurs de signaux sont utilisés pour augmenter le signal au fur et à mesure que le temps (et donc la profondeur de l’écho) s’écoule à partir de l’instant d’émission. Cela porte le nom de « correction de gain en fonction de la profondeur » ou encore time gain control (TGC).
Enfin, il faut bien garder à l’esprit que le temps nécessaire à l’émission-réception des échos successifs est très court, permettant d’obtenir l’information désirée en très peu de temps. À titre d’exemple, calculons le temps nécessaire pour construire une ligne échographique dans une exploration sur une profondeur de 15 cm. Le temps nécessaire pour l’arrivée des échos les plus profonds est :
t = 2d / c donc t = 2 · 0,15 m / 1500 m·s-1 = 200 . 10-6 s = 200 μs
Réalisation d’une image en mode B
La fabrication d’une image numérique consiste à obtenir suffisamment d’informations pour attribuer une valeur à chaque pixel. Nous venons de voir que la réalisation d’un tir puis l’analyse des échos permettaient de collecter les valeurs d’échogénicité pour chaque profondeur située le long de la ligne de tir. Si l’on multiplie les émissions de façon incrémentale le long de la sonde, on réalise un balayage par les lignes de tir d’une surface plane à l’intérieur du patient (une coupe) (figure 7.6).
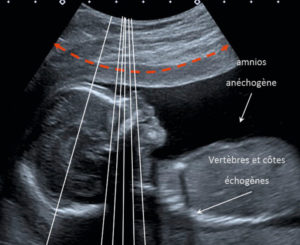
Image échographique et représentation schématique des lignes d’acquisition (lignes blanches) ayant effectué le balayage figuré par la double flèche rouge.
L’image obtenue (coupe sagittale d’un fœtus) correspond à l’ensemble de ce qui a été balayé par les tirs ultrasonores.
Par convention, la lecture d’une image échographique est toujours la même (voir chapitre 2) :
- la sonde est située en haut de l’image ;
- la forme de la sonde détermine celle de la partie haute de l’image échographique. Sur la figure 7.6, il s’agit d’une sonde courbe, ce qui explique la courbure du haut de l’image. Si la sonde avait été droite, le haut de l’image aurait été rectiligne ;
- les échos les plus profonds sont en bas de l’image ;
- si la sonde est placée de façon à obtenir un plan de coupe transversal, la droite réelle (du patient) est située à gauche de l’image et la gauche réelle est placée à droite de l’image. Si la sonde est dans une position sagittale ou oblique, les régions les plus crâniales se trouvent sur la gauche de l’image, et les régions les plus caudales sur la droite de l’image. Cela permet à chacun de comprendre l’orientation de la sonde en regardant l’image.
Comment sont créés les niveaux de gris dans une image échographique ? Très simplement, on représente, après la correction de gain en fonction de la profondeur, l’amplitude de chaque écho reçu par un niveau de gris et on attribue ce niveau au pixel correspondant à la localisation de l’écho. Les échos faibles sont par convention représentés par un gris presque noir et les échos puissants sont représentés par des niveaux de gris plus proches du blanc. La gamme d’amplitude possible des échos étant extrêmement vaste, on ne peut pas la représenter entièrement car son étendue dépasse les capacités de la vision humaine (qui ne peut distinguer guère plus de 20 à 30 niveaux de gris différents sur une même image). On utilise donc, comme le font nos sens naturels d’ailleurs, une conversion via une échelle logarithmique avant de représenter l’image en échelle de gris. Ces paramètres de conversion sont bien entendu accessibles à travers les réglages de la machine. Typiquement, on représente sur une même image une gamme d’échos, appelée aussi gamme dynamique, d’au moins 60 dB (décibels), c’est-à-dire une amplitude 1000 fois plus forte pour l’écho qui sature le blanc que pour l’écho donnant le premier niveau de gris. On appelle cette image une échographie en mode B, B pour brillance.
Finalement, une échographie en mode B est une cartographie du plan de coupe choisi, représentant les contrastes d’impédance acoustique des tissus rencontrés. Ces variations d’impédance sont liées à des changements, de faible ampleur, de la masse volumique ou de l’élasticité des tissus. Elles sont assez fortement corrélées à l’anatomie et on parle donc d’écho-anatomie pour traduire l’aspect des organes explorables sur ces images. Pour être précis, notons aussi que l’image obtenue se situe dans le plan de coupe passant par la sonde et formé par l’ensemble des faisceaux acoustiques ; d’où le terme d’échotomographie que l’on rencontre parfois, fondé sur la racine grecque « tomo » pour coupe.
Le balayage des lignes acoustiques produit une coupe. Le nombre d’images produites par seconde est appelé « cadence image ». À quelle cadence obtient-on les images du mode B ? Reprenons l’exemple précédent où l’acquisition d’une ligne nécessitait 200 μs. On peut donc disposer de 5000 lignes par seconde. Considérons qu’une image de qualité se compose de 200 lignes échographiques. On peut réaliser 5000/200, soit 25 images par seconde. Cette technique possède donc des cadences proches de celle du cinéma ou de la vidéo, et permet ainsi une acquisition dite en « temps réel ». C’est un avantage majeur de ce type d’imagerie.
Mode temps-mouvement (TM)
Ce mode appelé TM fut d’emblée inventé pour l’exploration cardiaque avant même la généralisation du mode B. Le cœur étant, par définition, une structure mobile, il est possible d’explorer les mouvements des parois ou des valves à l’aide d’une seule ligne immobile traversant des structures mobiles le long de cette ligne d’exploration.
Comme on le voit sur la figure 7.7, on utilise maintenant le mode B pour bien positionner la ligne du mode TM (pointillée). À la demande, le balayage est arrêté et on voit défiler le temps sur l’axe horizontal, ce qui permet d’analyser finement la dynamique temporelle des mouvements antéropostérieurs des structures croisant la ligne TM.
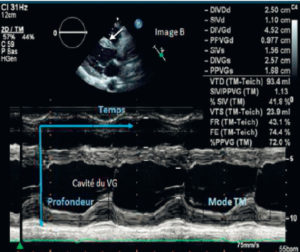
Sur cette copie d’écran, on voit en haut une image mode B du cœur qui a servi à positionner la ligne du mode TM (flèche).
Le résultat apparaît en bas, le temps en abscisse et la profondeur en ordonnée. Ce mode permet de mesurer notamment l’épaisseur des parois et le diamètre de la cavité ventriculaire gauche en systole et en diastole.
Mode 3D
L’opérateur peut déplacer le plan de coupe du mode B à sa guise et explorer ainsi l’anatomie de la région d’intérêt en trois dimensions, mais la représentation tridimensionnelle n’existe alors que dans le cerveau de l’échographiste. Cela demande une compétence forte et ne laisse pas de trace objective. On a donc imaginé piloter les faisceaux ultrasonores dans toutes les directions de façon à proposer une acquisition tridimensionnelle. La première méthode fut de placer une sonde barrette bidimensionnelle ordinaire dans un boîtier équipé d’un moteur faisant pivoter cette sonde lentement. Les acquisitions planes ainsi accumulées et mises en mémoire permettent ensuite de reconstituer un volume 3D et de proposer des visions selon différents angles. Avec cette technique, le caractère temps réel de la technique est perdu.
D’autres technologies ont vu le jour plus récemment, notamment pour les besoins de l’échocardiographie et de l’échographie obstétricale, comme dans l’exemple de la figure 7.8. Elles utilisent des sondes plus complexes, formées de capteurs ayant une structure matricielle de plus de 3000 éléments indépendants. Elles sont ainsi capables d’envoyer des tirs ultrasonores dans un volume. Des électroniques de pilotage adaptées ont été développées et permettent de saisir des volumes 3D avec un bon niveau de résolution spatiale et une cadence image satisfaisante.
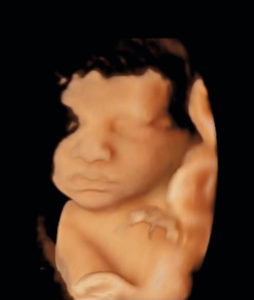
Technologie 3D, extraction de la surface cutanée in utero d’un fœtus (âge gestationnel : 35 semaines d’aménorrhée).
Bases sémiologiques du mode B
Comme nous l’avons indiqué au paragraphe « Réalisation d’une image en mode B », l’affichage des images suit les règles classiques de l’imagerie médicale. La gauche du patient est à droite de l’image et, pour les coupes sagittales, le haut du patient est à gauche de l’image. Par ailleurs, le nez de sonde au contact avec le patient est positionné classiquement en haut de l’écran.
Échogénicité
Rappelons que l’image échographique en mode B est la représentation de l’intensité des échos ayant pris naissance tout au long de la propagation des faisceaux. On parle d’échogénicité. Si on revient à l’origine physique, c’est une carte des différences d’impédance acoustique de la zone explorée. Cela explique une caractéristique fondamentale de ces images : les zones parfaitement homogènes ne produisent pas d’écho. Elles sont dites anéchogènes, c’est-à-dire sans écho. Elles apparaissent en noir. Les structures vraiment homogènes sont les liquides purs. Les tissus, a contrario, sont parcourus de travées de collagènes, de microvaisseaux, de cellules, qui elles-mêmes possèdent un noyau et des microstructures internes responsables d’une diffusion plus ou moins forte des ultrasons. Les liquides donnant lieu à des plages anéchogènes sont donc le liquide amniotique (voir figure 7.6), la bile, l’urine, le liquide cérébrospinal (LCS) visible en échographie transfontanellaire (à travers les fontanelles des nouveau-nés) en pédiatrie. Les épanchements pleuraux, péricardiques ou péritonéaux, les kystes simples sont aussi des zones anéchogènes et cela contribue d’ailleurs à leur identification. Le cas du sang est à distinguer : ce n’est pas un liquide à proprement parler car il contient 4 à 5 millions d’hématies par millimètre cube. Aux fréquences usuelles de 2 à 12 MHz, cela entraîne une diffusion extrêmement faible par rapport aux échos provenant des autres tissus. La conséquence est que le sang apparaît en noir sur les réglages usuels. Le repérage des gros vaisseaux, ainsi clairement identifiables, constitue d’ailleurs une des bases de l’échoanatomie. Néanmoins, cette diffusivité acoustique du sang donne des signaux, certes faibles, mais qui permettent la construction des modes Doppler (voir plus loin). Notons aussi que les globules rouges sont parfois regroupés en amas de rouleaux voyageant ensemble ; c’est le cas lorsque le cisaillement de l’écoulement est faible. Le centre diffuseur est alors beaucoup plus efficace et plus échogène ; le sang devient visible en échographie classique, par exemple dans la veine cave inférieure ou au sein d’un atrium gauche dilaté.
Les fortes ruptures d’impédance acoustique entraînent des échos très puissants qui sont codés en blanc sur les images. Les interfaces ayant un coefficient de réflexion proche de 100% entraînent une réflexion totale du faisceau : le faisceau émis ne poursuit pas l’exploration à des profondeurs plus grandes. On obtient alors un écho saturé en blanc, hyperéchogène, et en arrière une zone sans écho ou contenant des artefacts. Les structures osseuses et les organes à contenu gazeux (poumons et tube digestif) produisent de telles situations et constituent donc une limite à l’exploration échographique.
Cône d’ombre et renforcement postérieurs
Nous avons vu que l’amplitude des échos recueillis sur la sonde décroît avec la profondeur et que ce phénomène est compensé par une amplification à gain électronique croissant. Mais cela n’est juste qu’en moyenne. Plus spécifiquement, en arrière d’une zone plus atténuante, les échos sont de plus faible amplitude que leurs homologues de même profondeur et apparaissent avec une brillance affaiblie sous forme de cône d’ombre postérieur à la zone hyper-atténuante (figure 7.9). À l’inverse, un milieu moins atténuant (derrière une structure liquidienne comme un kyste) laisse passer un faisceau plus intense et les échos postérieurs paraîtront avec une brillance plus grande. On parle dans ce cas de renforcement postérieur.
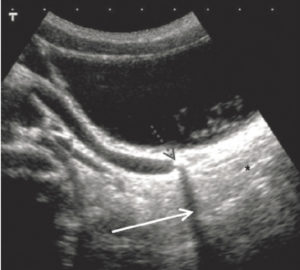
Formation d’artefacts.
Renforcement postérieur à droite de l’image (astérisque) en arrière de la zone liquidienne (vessie en réplétion). Cône d’ombre (flèche) situé en arrière d’un calcul de l’uretère (flèche pointillée).
Modes Doppler
Effet Doppler
L’effet Doppler, ainsi nommé d’après le nom du physicien autrichien Christian Doppler (1803–1853), traite des modifications de la fréquence des ondes perçues selon la vitesse relative de l’émetteur et du récepteur. Ce phénomène n’est pas limité aux ondes acoustiques ; c’est par exemple un moyen de mesure de la vitesse d’éloignement des galaxies par observation des décalages des spectres optiques.
Sur la figure 7.10, on a imaginé une situation banale : un véhicule se déplace en émettant un son à une certaine fréquence. Deux observateurs entendent le son du moteur, le premier, Mlle K., voit la machine s’éloigner, tandis que M. J. la voit se rapprocher de lui. On a noté T0 la période du son et λ0 sa longueur d’onde lorsque la moto est au repos. V est la vitesse de déplacement horizontal. Les cercles qui sont dessinés en gris représentent les fronts d’onde (ou zone équiphase). Ils ne sont pas concentriques. En effet, le cercle le plus petit est le plus récent ; en revanche, le cercle le plus grand est plus ancien, c’est-à-dire qu’il a été émis auparavant, ce qui explique qu’il a eu le temps de grandir par propagation. Mais au moment de l’émission du plus grand cercle, la moto était plus à gauche ; le centre du grand cercle est donc décalé vers la gauche, et ce d’autant plus que l’engin se déplace vite. Le résultat est visible sans démonstration sur la figure 7.10 : M. J. perçoit des fronts d’onde tassés vers lui et donc la longueur d’onde qu’il entend est plus courte, ce qui correspond à une fréquence plus élevée : le son est plus aigu. Inversement, Mlle K. perçoit des fronts d’onde écartés ; elle entend un son plus grave. Cela décrit une expérience auditive courante quand nous sommes au bord d’une route et écoutons passer des véhicules à forte vitesse ; ils s’approchent avec un bruit plus aigu et s’éloignent avec un bruit plus grave. On peut facilement calculer de combien sont raccourcis ou écartés deux fronts d’onde successifs : le temps écoulé entre deux fronts est T0 et la distance parcourue par la moto est V.T0. Si, par convention, la vitesse V est comptée positive en situation de rapprochement et négative en situation d’éloignement, la longueur d’onde perçue par Mlle K. et M. J. est calculée par la même équation : λ = λ0 – V·T0. mais λ0 = c·T0 et donc λ = (1 – V/c)·λ0.
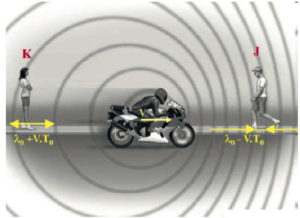
On voit sur ce schéma une source de son en déplacement, le moteur de la moto, et deux observateurs, Mlle K. et M. J.
Pour calculer la fréquence, il suffit de considérer que f = c/λ. Si V/c est petit devant 1, le calcul se simplifie et aboutit en première approximation à f = f0· (1 + V/c).
On voit que f est égal à f0 additionné d’un petit terme égal à f0· V/c. C’est ce que l’on appelle le décalage Doppler de fréquence fD. La fréquence Doppler fD est la différence entre la fréquence perçue par l’observateur avec celle émise par l’émetteur. De façon simple, elle répond à l’équation suivante :
fD / f0 = V / C
Le rapport des fréquences (Doppler et originelle) est égal au rapport des vitesses (objet et onde). À cause de la simplification effectuée dans le calcul, cette loi n’est valide que pour les vitesses V petites devant c. La fréquence fD a le même signe que V : positif en rapprochement et négatif en situation d’éloignement.
Mode Doppler continu
Le décalage de fréquence lié à la vitesse de déplacement est mis à profit pour effectuer à distance des mesures de vitesse, avec les radars par exemple. En médecine, ce décalage est surtout utilisé pour mesurer la vitesse du sang.
Sur la figure 7.11, on voit le principe de fonctionnement d’un système Doppler continu. La sonde émet un faisceau en permanence à la fréquence f0, d’où l’appellation Doppler à émission continue, et capte simultanément les ondes rétrodiffusées. Les ondes rétrodiffusées par les globules rouges subissent deux fois l’effet Doppler, une première fois lorsque les hématies sont éclairées par le faisceau en s’en éloignant (comme sur la figure) et une seconde fois lorsqu’elles deviennent à leur tour émettrices en direction de la sonde. Cela explique le facteur 2 que l’on trouve dans le calcul. La vitesse relative entre la sonde et les hématies n’est pas la même que la vitesse du sang car le vaisseau est oblique par rapport à la sonde. La vitesse « vue » par la sonde est donc la projection de la vitesse réelle des hématies sur la ligne du faisceau ultrasonore. Elle se calcule en multipliant V (la vitesse réelle des hématies) par le cosinus de l’angle θ entre le vaisseau sanguin et la ligne de tir ultrasonore. De façon réciproque, lorsqu’on veut utiliser l’effet
Doppler pour mesurer une vitesse de circulation sanguine, on mesure fD connaissant f0 et cos θ et on déduit V grâce à :
V = (fD / f0) * c / {2⋅ cos θ}
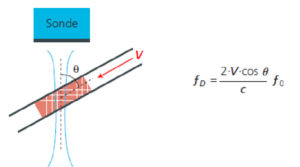
Schéma de fonctionnement du mode Doppler continu.
Une sonde engendre un faisceau ultrasonore dessiné en bleu qui croise un vaisseau sanguin sous l’angle θ. La vitesse de circulation est indiquée par le vecteur V.
On comprend donc que si le vaisseau sanguin est strictement perpendiculaire à la sonde (angle θ = π/2), il n’existe pas de signal Doppler (cos θ = 0 donc fD = 0). À l’inverse, si le vaisseau est exactement dans l’axe du faisceau ultrasonore et donc perpendiculaire à la sonde, cos θ vaut 1 et la fréquence Doppler est maximale.
Mode Doppler pulsé
L’inconvénient majeur du Doppler à émission continue est qu’il n’existe pas de discrimination en fonction de la profondeur. Ces systèmes sont donc très simples et faciles à utiliser pour des vaisseaux superficiels facilement repérables en fonction des repères anatomiques. On peut par exemple très aisément utiliser un petit appareil portatif aux urgences pour contrôler la perméabilité des axes vasculaires des membres en cas de suspicion de thrombose.
En revanche, si l’on veut apprécier l’hémodynamique d’une artère rénale ou d’un tronc porte en un point précis, il est nécessaire d’utiliser l’imagerie échographique en mode B pour positionner une zone dans laquelle on désire mesurer la fréquence Doppler (selon les mêmes principes que ceux exposés pour le Doppler continu). Cela est obtenu en utilisant une émission pulsée produite de façon à analyser précisément une profondeur donnée en utilisant le délai nécessaire aux ondes acoustiques pour parcourir un aller-retour. Tout ce qui est situé en dehors de cette zone Doppler d’intérêt n’est pas analysé. La multiplication des tirs permet d’obtenir l’évolution temporelle des vitesses dans cette zone.
Si le signal Doppler pulsé permet une parfaite localisation du flux en profondeur, il a l’inconvénient d’être limité dans la fréquence mesurable. En effet, les allers-retours successifs des impulsions ultrasonores se font à une fréquence forcément limitée. Cette fréquence d’échantillonnage limite la fréquence Doppler mesurable et donc les vitesses d’écoulement sanguin mesurables. Cette limitation s’accroît en profondeur et avec la fréquence des ultrasons utilisés. Le Doppler continu, lui, n’a pas de limitation en fréquence et permet de mesurer toutes les vitesses d’écoulement.
Représentation du signal Doppler
La nature faisant bien les choses, en utilisant les fréquences habituelles de l’échographie (quelques MHz) et avec le rapport V/c vitesse du sang sur vitesse des ultrasons typiquement compris entre 1/10 000 et 1/1000, la fréquence des signaux Doppler est dans la gamme du kHz et donc bien adaptée à notre audition. Le signal Doppler s’écoute donc, ce qui permet d’ajuster finement le positionnement manuel de la sonde et de la zone de mesure.
Par ailleurs, il existe des dizaines de millions d’hématies circulantes possédant des vitesses différentes et engendrant donc tout un spectre de fréquences Doppler. Cela peut être rendu très explicite en utilisant l’outil mathématique de la transformée de Fourier qui décompose les différentes fréquences contenues dans un signal pendant une durée d’analyse définie. On obtient ce que l’on appelle un spectre Doppler représentant la part respective des différentes vitesses contenues dans le signal de la zone d’intérêt. C’est l’analyse dite « spectrale ». C’est ce mode qui est représenté sur la figure 7.12.
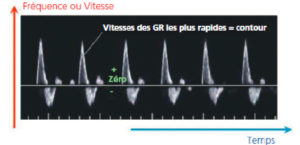
Analyse de spectre d’un signal Doppler, ici obtenu sur une artère fémorale.
Le temps est en abscisse, les fréquences positives ou négatives en ordonnée et l’échelle de gris montre la puissance du signal Doppler pour chaque pixel. L’hémodynamique est bien restituée en termes de fluctuation temporelle des vitesses. GR : globules rouges.
Un apport intéressant de l’analyse spectrale est qu’elle met parfaitement en évidence les vitesses maximales circulantes, le plus souvent au centre du vaisseau. Elles donnent lieu aux fréquences les plus élevées, en positif ou en négatif, et le contour du spectre permet de parfaitement suivre l’hémodynamique, même lorsque le rapport signal sur bruit est faible dans l’exploration des vaisseaux profonds.
Mode imagerie Doppler
En combinant la technique de l’imagerie qui permet un balayage d’un plan de coupe et la capacité du Doppler pulsé de réaliser des mesures de vitesse sur une zone restreinte et assez bien résolue (de l’ordre de quelques longueurs d’onde), il est possible de créer un mode cartographique en temps réel des vitesses circulatoires sur une zone d’exploration définie par l’opérateur. Les vitesses de circulation sont représentées en couleur avec pour convention : nuances de rouge pour les flux se rapprochant de la sonde et nuances de bleu pour les flux s’en éloignant. On parle communément de mode Doppler couleur. Cette carte de couleurs peut être actualisée avec une cadence assez rapide (typiquement 5 à 30 fois par seconde) tout en la superposant à l’affichage de l’image en l’échelle de gris du mode B (figure 7.13).
On voit sur la figure 7.13 une image figée résumant une acquisition couplant trois modes. Le mode B permet de repérer la lumière des vaisseaux carotidien et jugulaire interne. Le mode couleur représente la circulation sanguine dans la zone d’intérêt (cadre oblique) et le signal Doppler pulsé est affiché en dessous sous forme d’analyse spectrale où l’on distingue cinq cycles cardiaques. Elle donne la distribution des vitesses au point d’intersection des lignes blanches dans l’artère carotide. Le contour spectral montre les vitesses maximales des hématies circulantes dans la zone de mesure positionnée au centre de l’artère. On remarque que les tirs ultrasonores pour les modes Doppler ont été inclinés par rapport au capteur situé en haut de l’image mode B au contact de la peau (la ligne blanche et la boîte Doppler sont obliques). Cela permet de diminuer l’angle entre l’axe des vaisseaux et les tirs Doppler, et ainsi d’obtenir une valeur plus grande du cosinus de cet angle, permettant une évaluation plus fidèle des vitesses. Par convention, la tête du patient est du côté gauche de l’image ; le sang artériel carotidien circule de la droite vers la gauche, se rapprochant donc de la sonde. Cela explique le codage en rouge du flux carotidien.
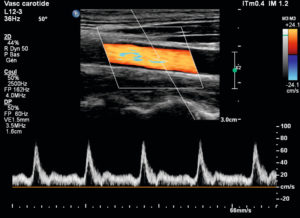
Aspect habituel d’une image associant les modes B, imagerie Doppler et spectre du Doppler pulsé.
Le signal Doppler pulsé a été recueilli dans la fenêtre de mesure au centre de l’artère carotide commune encodée ici en rouge orangé. L’écoulement se fait de la droite vers la gauche de l’image, donc en situation de rapprochement de la sonde. Le codage en bleu au centre correspond pour quelques pixels à un artefact de sous-échantillonnage.
Agents de contraste échographiques
Principes des microbulles
Les échographistes disposent depuis les années 2000 d’agents de contraste injectables en intraveineux. Il s’agit de suspensions de microbulles de gaz stabilisées de diamètre de 1 à 5 μm. Ces agents restent en circulation une dizaine de minutes. En revanche, à la différence des agents de contraste utilisés en TDM et en IRM, les microbulles de gaz ne diffusent pas dans le tissu interstitiel. Ce sont des agents strictement intravasculaires. Après plusieurs minutes, les bulles sont détruites et le signal décroît. Le gaz contenu dans les bulles est éliminé par voie respiratoire.
Sous l’effet du faisceau ultrasonore qui les frappe, les microbulles entrent en résonance, c’est-à-dire qu’elles se contractent et se dilatent selon la fréquence de résonance. Ce faisant, elles se comportent chacune comme un petit émetteur/amplificateur local. La somme de tous les petits signaux créés par chaque bulle produit un signal non linéaire. De manière très simple, les bulles qui entrent dans le champ de vue du faisceau ultrasonore « brillent » de manière très intense, produisant un contraste marqué entre les zones où elles sont situées (vaisseaux) et les zones où elles ne le sont pas. Aux niveaux d’énergie habituellement utilisés pour réaliser une échographie morphologique, les bulles se dilatent trop et éclatent instantanément ; l’énergie du faisceau est donc diminuée. La conséquence est qu’il n’est pas possible de réaliser une échographie morphologique avec ce mode. Sur les échographes modernes, il est possible d’afficher sur l’écran à la fois une image morphologique de repérage et l’échographie de contraste pour naviguer dans les deux à la fois.
L’analyse d’une échographie de contraste prend en compte la manière avec laquelle les structures d’intérêt sont modifiées par l’arrivée du produit de contraste : augmentation de la brillance (rehaussement ou, en langage commun, « prise de contraste »), comparaison entre deux structures proches, évolution dans le temps.
Effets indésirables et contre-indications
Les produits de contraste ultrasonore sont très bien tolérés. Ils ne sont pas néphrotoxiques et peuvent être utilisés en cas d’insuffisance rénale. Ils ne sont pas autorisés pendant la grossesse. Ils ne doivent pas être utilisés en cas d’infarctus du myocarde récent ou d’insuffisance respiratoire sévère.
Bases technologiques
Capteurs ou sondes d’échographie
Comme collecteurs de signaux, les sondes (ou capteurs) sont des éléments déterminants de la qualité des images obtenues. Ce sont aussi les objets que les échographistes tiennent dans leur main et appliquent sur les patients. Voyons ci-après le type de capteurs qui est à la base du développement des imageurs modernes : il s’agit de sondes à barrette de transducteurs. Elles sont schématisées dans la figure 7.14.
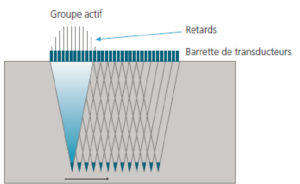
Un alignement ou barrette de transducteurs indépendants est piloté par le même nombre de systèmes électroniques émetteur-récepteur qui déterminent l’ordre temporel d’émission (retard).
On peut ainsi combiner à volonté les ondes élémentaires créées par chaque transducteur et modeler la forme et la direction du faisceau ultrasonore.
On peut ainsi combiner à volonté les ondes élémentaires créées par chaque transducteur et modeler la forme et la direction du faisceau ultrasonore.
D’une manière générale, on appelle transducteur un dispositif capable de convertir un signal physique en un autre. Dans le cas de l’échographie, les transducteurs sont formés d’un matériau piézoélectrique capable de transformer une impulsion électrique en un microdéplacement conduisant à la création d’une onde acoustique. Réciproquement, une onde sonore frappant la surface d’un transducteur est transformée en une impulsion électrique. Une sonde d’échographie est formée par l’association de nombreux transducteurs de base, indépendants les uns des autres. Pour piloter à volonté les faisceaux ultrasonores, à la fois en termes de focalisation et d’orientation, on adresse à chaque transducteur d’une barrette un signal adéquat qui l’active. Chaque transducteur produit alors une petite onde et c’est la combinaison cohérente de toutes les ondes créées par les transducteurs qui forme le faisceau ultrasonore final. En modifiant l’amplitude et le retard avec lesquels chaque transducteur est activé, il est possible de déterminer le point où les ondes se rejoignent et se recombinent. On parle de point focal. De même, en déplaçant, comme on peut le voir sur la figure 7.14, le groupe actif de transducteurs, il est possible d’obtenir une translation du faisceau explorant les tissus. La polyvalence de ces barrettes permet, via l’électronique de pilotage, la genèse d’impulsions brèves, la focalisation de l’énergie acoustique sur quelques longueurs d’onde et le balayage de la ligne d’exploration. Ce sont les ingrédients nécessaires à la réalisation des images mode B 2D et 3D.
Conclusion
Caractéristiques générales de l’échographie
Les éléments déterminant les aspects spécifiques de l’échographie peuvent être résumés de la façon suivante.
- Avantages :
- investigation non ionisante sans limitation de dose ;
- exploration en temps réel ; l’opérateur est en situation de piloter la sonde dans l’espace anatomique 3D du patient ;
- cadence élevée de renouvellement des images, précieuse en cardiologie ou pour les explorations dynamiques de l’appareil musculosquelettique ;
- excellente résolution spatiale ;
- examen au contact du patient, prolongement naturel de l’examen clinique du patient ;
- technique légère et mobile, qui peut être réalisée facilement au lit du patient ou au bloc opératoire ;
- guidage des actes de biopsie percutanée ou de ponction vasculaire ;
- coût d’investissement moindre que la TDM, l’IRM ou la scintigraphie.
- Limites :
- exploration limitée par les structures contenant des gaz (digestives, pulmonaire) et le squelette ;
- exploration limitée dans l’espace, différente en ce sens des autres techniques d’imagerie en coupe où l’on acquiert un volume anatomique prédéfini mais large ;
- demande un long apprentissage (courbe d’apprentissage) pour acquérir la coordination main-regard-analyse des images ;
- variabilité de la qualité des images en fonction des patients. L’échographie cardiaque d’un patient obèse et porteur d’une bronchopathie chronique obstructive est de moins bonne qualité que celle d’un jeune sportif de 60 kg ;
- il existe, comme pour toutes les modalités d’imagerie, des artefacts qu’il faut connaître et interpréter ;
- une exploration échographique est moins réinterprétable en différé que les images en coupe, car plus dépendante de la qualité de l’acquisition et du stockage des données. Cet aspect est moins problématique depuis la généralisation des systèmes de stockage d’images (PACS) et la possibilité d’acquérir et de stocker des boucles vidéo.
Perspectives d’avenir
Les technologies à l’œuvre dans la conception et la fabrication des échographes ont continuellement évolué depuis l’époque des pionniers de l’échographie des années 1960 et 1970. Les progrès de la miniaturisation et de la micromécanique permettent de produire des sondes de plus en plus performantes. Par ailleurs, les composants électroniques actuels permettent de s’approcher très près des limites théoriques du rapport signal sur bruit. Les machines sont numériques depuis la fin des années 1980 et celles d’aujourd’hui comportent des microprocesseurs extrêmement puissants qui supportent les algorithmes très sophistiqués de traitements de signaux et d’image qui interviennent dans les calculs d’optimisation.
Les usages se diversifient : il est commode et sécurisant de disposer d’un outil échographique dans de nombreux lieux comme les réanimations, les urgences, les salles d’anesthésie locorégionale, les lieux de biopsie ou de prélèvement de tissus.
En termes de sécurité, nous disposons d’un recul suffisant (en particulier avec des millions d’échographies anténatales) permettant d’affirmer qu’il s’agit d’une méthode sans danger. Toutefois, les ultrasons interagissent avec les tissus et, à forte intensité, peuvent créer des effets biologiques significatifs. Un nouveau secteur est aujourd’hui en plein développement ; il s’agit de l’utilisation des ultrasons à but thérapeutique. Des machines sont déjà commercialisées qui permettent une ablathermie ou destruction localisée des tissus via l’échauffement jusqu’à 60 à 90 °C de la cible pendant quelques secondes, cela grâce à un faisceau ultrasonore fortement focalisé et de haute intensité. Les lésions prostatiques ou les fibromes utérins constituent deux exemples des premières applications validées. Le traitement du glaucome chronique et le traitement de cibles tumorales font l’objet d’essais cliniques de grande ampleur. D’autres voies de recherche visent à augmenter de manière très sensible la biodisponibilité locale d’agents anticancéreux, ouvrant la possibilité de limiter les effets toxiques sur l’ensemble des organes.
Enfin, les années à venir verront la généralisation des échographes ultraportables qui tiennent dans la poche d’une blouse ou ont la dimension d’une tablette informatique. Le défi associé à cette diffusion n’est pas technologique ou commercial, mais celui de la formation des futurs utilisateurs.
Essentiel à retenir
- Les ondes ultrasonores utilisées en médecine sont des ondes mécaniques de 2 à 20 MHz dont la longueur d’onde au sein des tissus est de quelques dixièmes de millimètre.
- La célérité et la masse volumique des tissus mous varient très légèrement et cela suffit à créer des modifications d’impédance acoustique génératrices d’échos acoustiques.
- La mise en forme et le traitement numérique des échos recueillis permettent la reconstitution d’images et de cartographies de vitesses grâce à l’effet Doppler.
- Les modes associés à l’effet Doppler apportent une information fonctionnelle à l’exploration en montrant les mouvements du sang circulant.
- La vitesse du son dans les tissus est suffisamment rapide pour permettre une production d’images en temps réel.
- En tenant la sonde en main, l’échographiste est en situation de pilotage des plans de coupe qu’il va explorer au sein de son patient.
- Les systèmes échographiques bénéficient des dernières technologies en matière de science des matériaux pour les sondes et de puissance de calcul pour le traitement des signaux.
 |
Chapitre suivant |
 |
Retour au sommaire |
